华东医药获Kiniksa两款自身免疫新药独家许可
新京报讯(记者张兆慧)2月23日,华东医药宣布,全资子公司中美华东已与Kiniksa签署独家许可协议,中美华东获得Kiniksa两款自身免疫领域的全球创新产品Arcalyst及Mavrilimumab,在中国、韩国、澳大利亚、新西兰、印度等24个亚太国家和地区(不含日本)的独家许可,包括开发、注册及商业化权益。
中美华东将向Kiniksa支付2200万美元首付款,最高不超过6.4亿美元的开发、注册及销售里程碑付款以及分级两位数的净销售额提成费。
Kiniksa是美国纳斯达克上市的全球性生物制药公司Kiniksa Pharmaceuticals,Ltd.的全资子公司,专注于发现、获取、开发和商业化调节免疫信号通路的治疗药物。此次涉及的两款产品均为自身免疫领域全球创新产品。
Arcalyst(Rilonacept)是重组二聚体融合蛋白,可阻断白细胞介素-1α(IL-1α)和白细胞介素-1β(IL-1β)的信号传导。Rilonacept最早由再生元公司研发,于2008年获得美国食药监局(FDA)批准,商品名为Arcalyst,用于治疗冷吡啉相关的周期性综合征,特别是家族性寒冷型自身炎症综合征和穆-韦二氏综合征。2020年,FDA批准其用于治疗IL-1受体拮抗剂缺乏症。
2017年,Kiniksa从Regeneron获得了Rilonacept的许可。Kiniksa开发Rilonacept用于治疗复发性心包炎适应症,一种自身炎症性的心血管疾病,主要症状表现为胸痛。2021年3月,Rilonacept获得FDA批准,用于治疗复发性心包炎,是FDA批准的第一款也是唯一一款适用于12岁及以上人群的治疗复发性心包炎药物。
Mavrilimumab是一种全人源单克隆抗体,可靶向粒细胞-巨噬细胞集落刺激因子受体α(GM-CSFRα),并抑制粒细胞-巨噬细胞集落刺激因子(GM-CSF)的信号传导。Kiniksa于2017年从MedImmune Limited获得Mavrilimumab的全球许可。Kiniksa正在准备开展Mavrilimumab用于GM-CSF相关的心血管疾病的海外Ⅱ期临床试验。
华东医药称,自身免疫及罕见病用药存在未被满足的临床需求和市场增长潜力,此次合作有利于公司加快推进创新国际化进程,持续深入布局免疫产品领域。
推荐阅读 相关文章
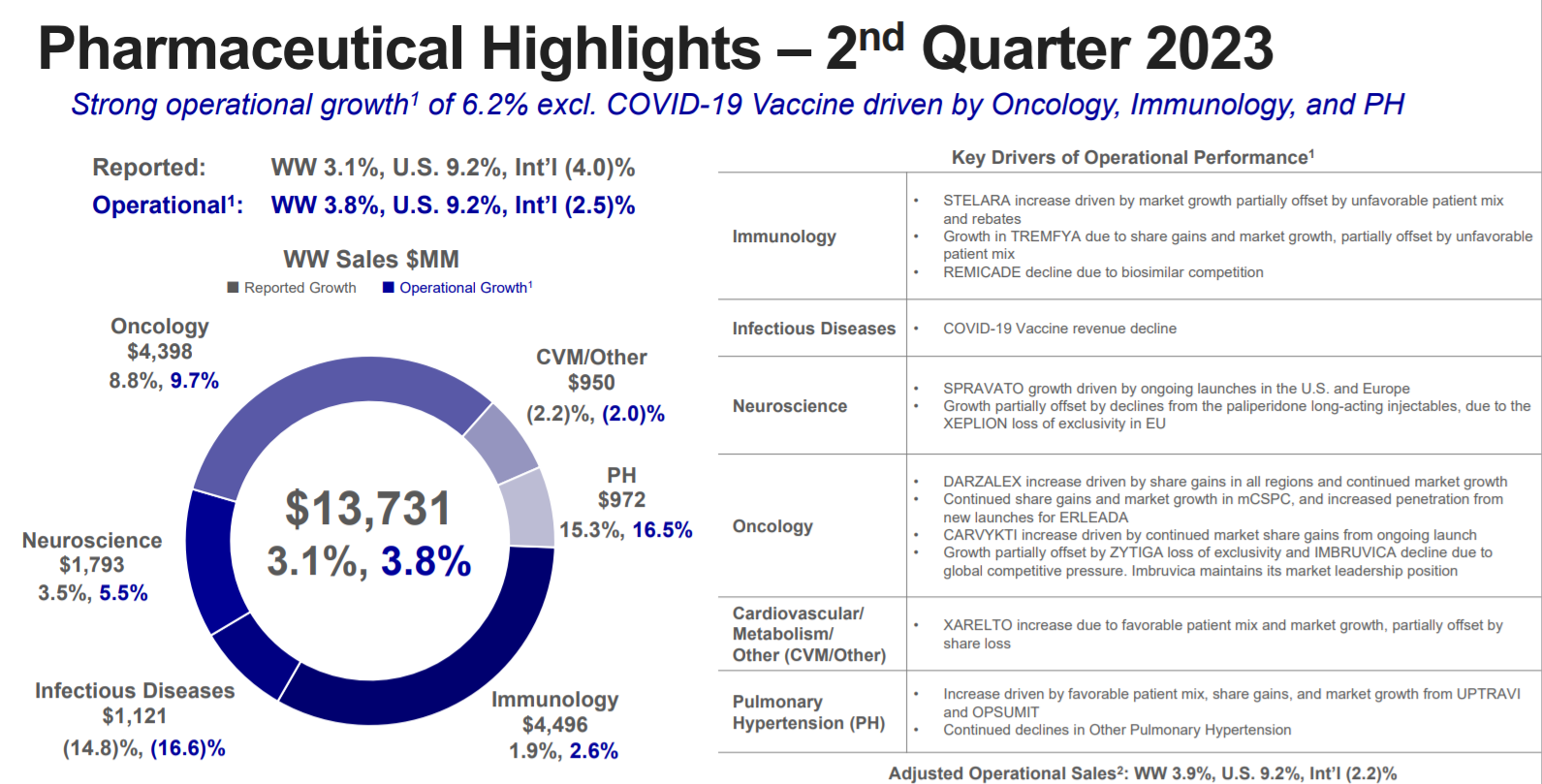
强生上半年营收503亿美元!Stelara超52亿美元,Darzalex增长22%
基于此,强生上调了2023年业绩预期,由原计划的979-989亿美元提高至993–1003亿美元。...
三年斩获6个IPO,中国药大悄悄跑出一个5千亿上市天团
对于生物医药这个特殊的行业,以及当前医药行业所面临的市场环境,不善于追逐热点但又执著且在不断沉淀的药大人来说,可能会在未来走得更远。...
价格炒至万元、网友购买受骗:渠道乱象下,进口新冠口服药物Paxlovid是否被“神”化?
谈及Paxlovid的适用人群,首都医科大学附属北京友谊医院药学部主任药师崔向丽表示,不是所有新冠阳性患者都需要这个药。...
第三批抗癌药品和罕见病药品可享增值税优惠
为鼓励制药产业发展,降低患者用药成本,财政部、海关总署、国家税务总局、国家药监局日前发布公告,发布第三批适用增值税政策的抗癌药品和罕见病药品...
国家药监局:加快新冠肺炎临床诊疗急需药品的审评审批
国家药监局副局长黄果20日在市场监管总局召开的涉疫药品和医疗用品稳价格保质量专题新闻发布会上表示,为了给疫情防控提供更多更好的“武器”,国家...
市场监管部门全力做好涉疫药品和医疗用品稳价保质
市场监管总局20日召开涉疫药品和医疗用品稳价格保质量专题新闻发布会,有关负责人表示,布洛芬、对乙酰氨基酚在产企业都在逐步释放产能,严厉打击涉...