君实生物医保谈判前夕遭狙击?前三季亏损11亿元
11月13日,上海君实生物医药科技股份有限公司(下称“君实生物”)发布“关于媒体报导的澄清公告”称,经核实,“公司认为该媒体文章关于本公司及有关人士的报道内容全面失实,与客观事实严重不符、相悖。”
此前一天,一篇名为《江湖就是人情世故》的文章在网络流传。该文章质疑君实生物研发的国内首个国产PD-1抗体药物特瑞普利单抗注射液,在不良反应发生率为97.7%的情况下有条件批准上市,还提及君实生物与礼来制药的合作、实控人无任何生物科学背景及研发实力与进度不匹配等问题。
随后,君实生物A股跌4%,H股跌4.52%。11月13日,君实生物A股跌6.22%,H股涨1.78%。与此同时,君实生物还收到上海证券交易所问询函,要求公司就相关文章涉及的问题于11月19日之前作出说明。
北京鼎臣医药管理咨询中心创始人史立臣对时间财经表示,该文章质疑君实生物的一个核心问题是,公司产品特瑞普利单克隆抗体注射液(商品名“拓益”)是有条件批准上市的,上市后需继续完成确证性临床研究,提交相应数据、材料等,以申请获得完全批准。如果君实生物已经在完善数据,或者已经完成了数据补充,则此事对君实生物的危急基本可以解除。如果没有,那么在新一轮医保谈判目录关键时期,君实生物就很难竞争得过正常上市的恒瑞、百济、信达等的产品。
对于不良反应发生率97.7%,史立臣认为,抛开级别谈不良反应的概率是不对的。不良反应分为五级:一级是轻度反应,二级是中度反应,到三级需临时停药,到四级五级就要停药,一级、二级的不良反应发生率超90%非常常见。文章把所有级别的不良反应发生率加起来,得出一个97.7%是无意义的。
时间财经多次联系君实生物方面,截至发稿时间,暂未获得回复。

核心产品遭质疑
君实生物成立于2012年,是一家创新型生物制药公司,产品覆盖肿瘤免疫治疗、代谢类疾病、炎症或自身免疫性疾病及神经系统疾病等多个领域,热门产品是肿瘤产品PD-1和新冠中和抗体产品。今年7月15日,公司登陆科创板,完成从新三板到港交所再到科创板的证券化之路。
君实生物此次被质疑的产品PD-1药物拓益(特瑞普利单抗注射液)是营收支柱。该产品于2018年12月17日获国家药监局有条件批准上市,是国内首个获批的国产PD-1单抗,主要用于治疗既往标准治疗失败后的局部进展或转移性黑色素瘤。
今年,该药联合阿昔替尼治疗黏膜黑色素瘤获得美国FDA孤儿药资格认定、用于鼻咽癌治疗、软组织肉瘤治疗的疗法分别获得美国FDA授予的孤儿药资格认定等,创下多个“国内第一”。
2019年1月,君实生物公布其PD-1药物拓益(特瑞普利单抗注射液)的价格为7200元/240mg(支),患者一年的使用成本约10万元,约为进口药的三分之一。
该产品于2019年2月底正式进入市场销售,2019年全年销售额达7.74亿元。进入2020年,特瑞普利单抗第一季度、第二季度分别实现销售收入1.72亿元、2.54亿元,在总营收中的占比超七成以上,毛利率89.84%。
对于安全性质疑,君实生物回应称,特瑞普利单抗注射液在获批适应症的安全性资料显示,特瑞普利单抗的适应症受试者数量为128人,三级及以上不良反应发生率为28.9%。
据国元证券数据,君实生物目前在研管线丰富,包括19个创新药和2个生物类似物。除了特瑞普利单抗,君实生物的JS002(PCSK9)正在进行III期临床试验的启动工作;JS016(中和抗体)海外针对轻型/普通型新冠肺炎患者的II期临床研究正在进行;JS108(重组人源化抗Trop2单抗-Tub196偶联剂)获得NMPA的IND批准。
对于被质疑的另一款代号为JS016的新冠病毒抗体药品,君实生物表示,美国礼来制药停止的ACTIV-3临床试验不涉及公司产品JS016。截至目前,JS016已顺利完成中国、美国2项健康受试者I期研究。在国内,由君实生物发起的一项在新冠病毒感染者中评价JS016初步临床疗效和安全性的国际多中心Ib/II临床研究仍按原计划进行。JS016同时正在美国开展1项由礼来制药发起的联合LY-CoV555的II期研究。

百亿市场
PD-1类药物是指不同于传统的化疗和靶向治疗,主要通过克服患者体内的免疫抑制,重新激活患者自身的免疫细胞来杀伤肿瘤,是一种全新的抗肿瘤治疗理念。
医药市场分析公司Evaluate Pharma预测,未来五年,肿瘤治疗药物仍然是全球市场销售中最好的领域。到2022年抗肿瘤药市场的规模预计将增长至1920亿美元,复合年均增长率达12.7%。
2018年被称为中国肿瘤免疫治疗元年,这一年的6月和7月,跻身全球十大畅销药物的“O药(纳武利尤单抗注射液)”、“K药(帕博利珠单抗注射液)”在国内获批上市。
君实生物PD-1特瑞普利单抗注射液是首个获批上市的国产PD-1产品,与之相差不到一个月上市的信达生物的信迪利单抗注射液,是第二个国产PD-1药物。
2019年,抗癌药物PD-1成为医保价格谈判最受关注的产品。当时默沙东、百时美施贵宝两家外企和君实生物、信达生物两家国内企业同台竞争,信达生物进入医保,君实生物未能如愿。
近期正值新一轮医保谈判目录关键时期,随着专家评审阶段结束,备受瞩目的谈判竞价即将启幕。君实生物的PD-1特瑞普利单抗成为今年PD-1品类入围的热门。
一年过去后,国内PD-1行业又添了四个对手:外资的罗氏、阿斯利康和国内企业百济神州、恒瑞医药。君实生物显然压力不小。
10月31日,君实生物披露的2020年三季报显示,报告期内实现营业收入10.11亿元,同比增长91.78%;归属于上市公司股东的净利润为-11.16亿元。其中,研发投入12.10亿元,同比增长97.19%。
君实生物表示,随着公司各项业务持续扩张和推进,短期内单产品的销售收入尚不能覆盖研发投入等费用支出,预计年初至下一报告期期末仍将亏损。
与此同时,今年1月1日开始进入医保的信达生物信迪利单抗,尽管该药品(10ml:100mg/瓶)从市场价超过7000元降至2843元,降幅超过60%,但今年上半年销售收入达到9.21亿元(同比增177.7%)。
据券商预测,国内PD-1市场高达百亿规模,还有数家国内公司研发的PD-1产品上市在即,这场PD-1竞争有望继续升级。
推荐阅读 相关文章
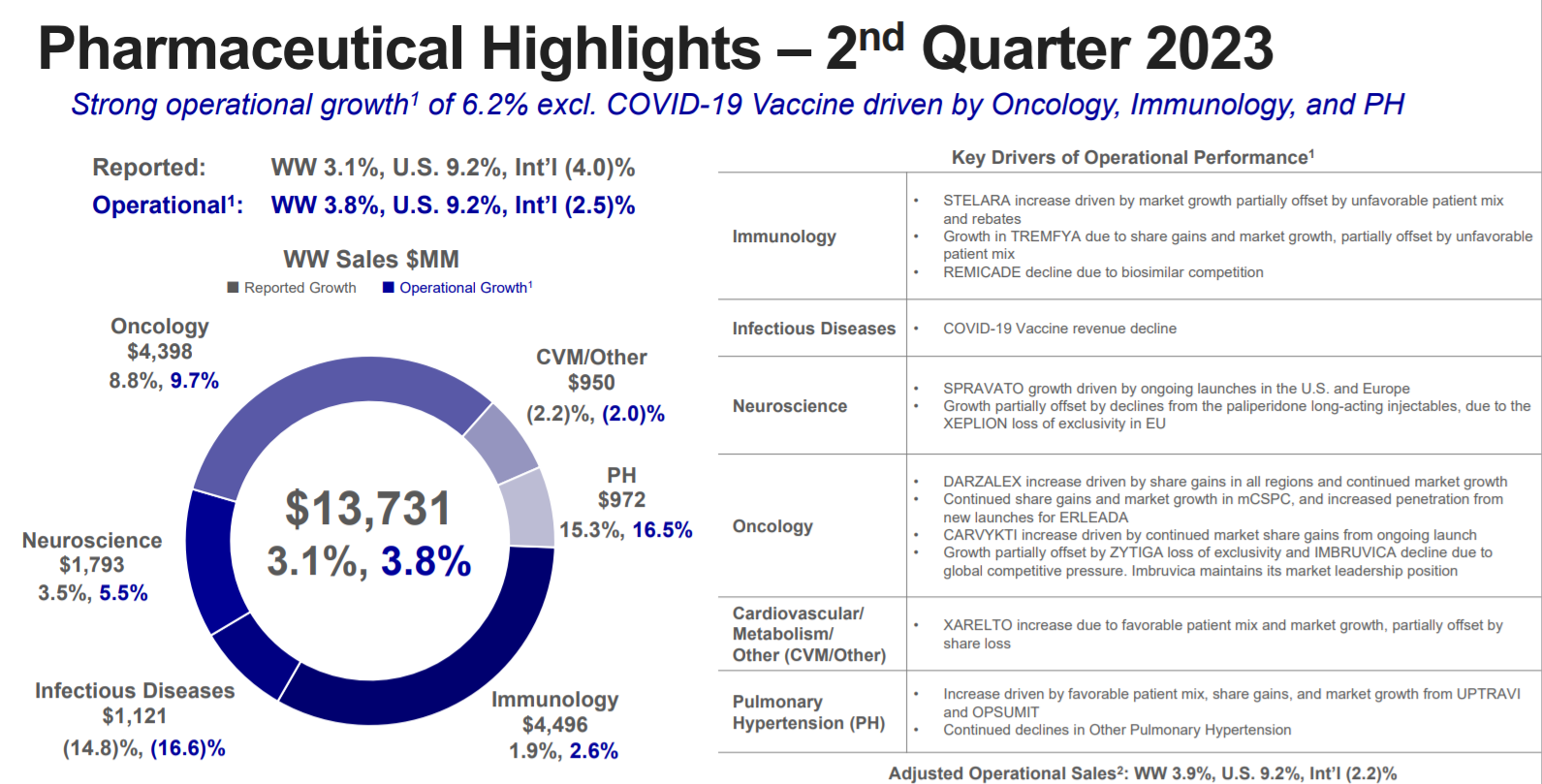
强生上半年营收503亿美元!Stelara超52亿美元,Darzalex增长22%
基于此,强生上调了2023年业绩预期,由原计划的979-989亿美元提高至993–1003亿美元。...
三年斩获6个IPO,中国药大悄悄跑出一个5千亿上市天团
对于生物医药这个特殊的行业,以及当前医药行业所面临的市场环境,不善于追逐热点但又执著且在不断沉淀的药大人来说,可能会在未来走得更远。...
价格炒至万元、网友购买受骗:渠道乱象下,进口新冠口服药物Paxlovid是否被“神”化?
谈及Paxlovid的适用人群,首都医科大学附属北京友谊医院药学部主任药师崔向丽表示,不是所有新冠阳性患者都需要这个药。...
君实生物登陆科创版:核心产品前途不明 盈利前景难料
值得注意的是,该公司目前尚未盈利,且仍处在巨亏之中,而其目前唯一被允许上市销售的药物——特瑞普利单抗已获批适应症所对应的市场规模较小,加上这...
君实生物火速收问询函 PD-1产品安全性遭质疑
一篇微信公号文章,让A+H未盈利创新药第一股君实生物(01877.HK/688180.SH)身陷舆论漩涡。11月12日,君实生物收到上交所问...
知名公众号发文质疑君实生物 是“躺枪”还是“石锤”
12日,微信公众号“兽楼处”发布一篇名为《江湖就是人情世故》的文章,这篇文章对生物医药公司君实生物的成立经过、药物研发时间、核心产品评审的合...
股价低开超5% 君实生物反驳自媒体安全性质疑
11月12日下午,有自媒体公众号发文质疑君实生物核心产品PD-1特瑞普利单抗(商品名“拓益”)的安全性,以及新冠中和抗体等多款在研产品存在问...
君实生物回复上交所:公众号有关报道内容全面失实
君实生物称,收到《问询函》后,公司进行了认真自查和核实。经确认,公司认为有关媒体报道中关于公司及有关人士的报道内容全面失实,与客观事实严重不...
君实生物回应新冠口服药物下半年申请上市:正在积极推进临床试验中
今日,据媒体报道,国内唯一获批进入临床试验的新冠治疗小分子药物VV116,年内通过临床试验后,将第一时间启动上市(NDA)申请。...