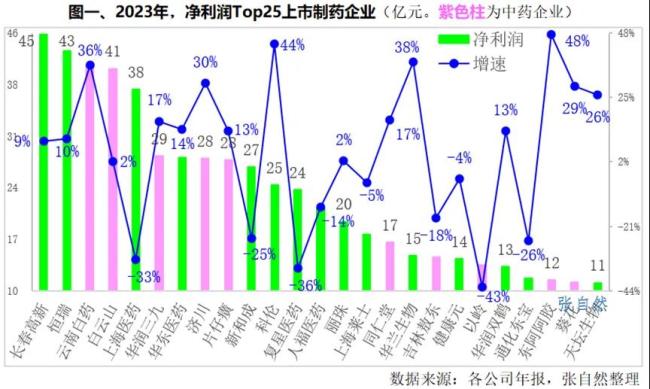
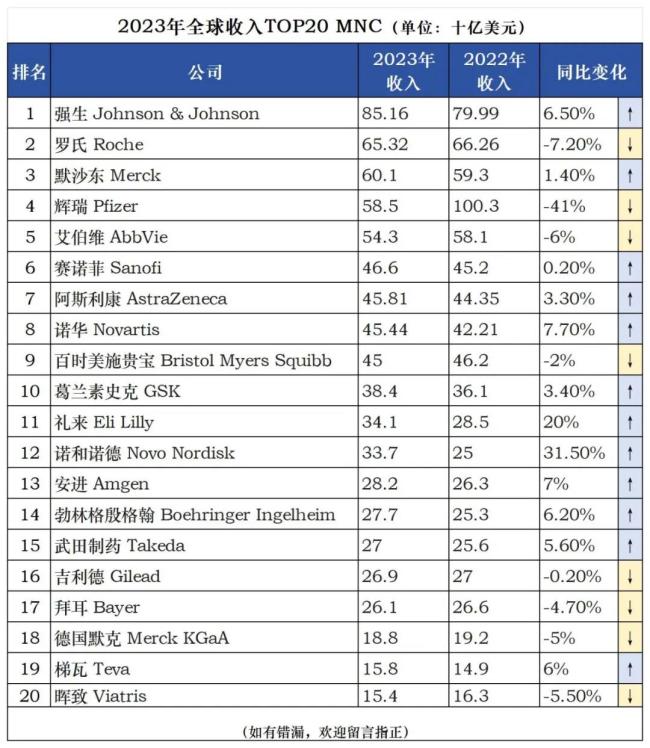
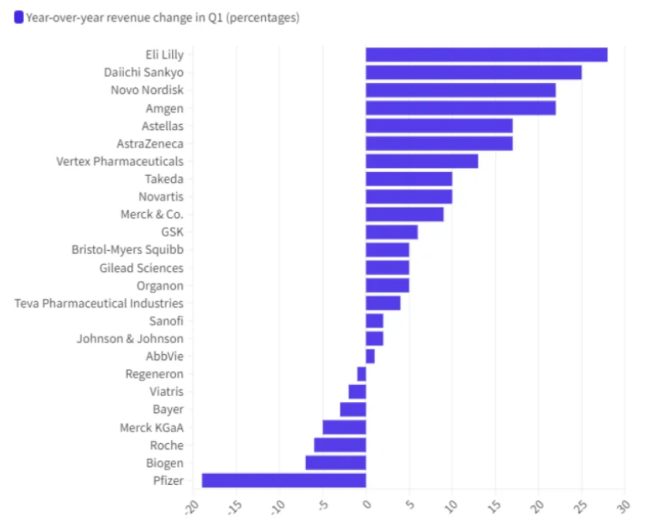
CDK4/6抑制剂三雄演义:诺华、礼来难分伯仲,辉瑞持续下滑,百亿美元市场谁是新王?(2)
在这样的背景下,近期举行的2024年ESMO大会上,NATALEE试验的4年结局更新成为了焦点。研究显示,瑞波西利+内分泌治疗相比对照组的治疗获益得到了延续且进一步增加,iDFS绝对获益从3年的3.1%增加至4年的4.9%(88.5% vs 83.6%,HR=0.715,P<0.0001)。在II期/III期、N0/N1-3等亚组患者中,同样观察到与总人群一致的获益趋势。该研究结果再次验证了瑞波西利+内分泌辅助强化治疗能显著降低HR+/HER2-早期乳腺癌复发风险,同时也进一步表明瑞波西利治疗获益并非由任何特定亚组驱动,其获益人群具有广泛性。
得益于NATALEE临床试验的积极结果,瑞波西利赢得了FDA对其在早期HR+/HER2-乳腺癌辅助治疗中的批准。这标志着瑞波西利在治疗HR+早期乳腺癌方面的潜力和价值正逐渐被医疗界认可和证实。
特别值得一提的是,瑞波西利的新适应症覆盖了那些没有淋巴结癌细胞转移的患者群体,这与礼来的阿贝西利有所不同,后者在HR+/HER2-乳腺癌的批准仅限于有淋巴结受累的患者。这一区别使得瑞波西利在治疗早期乳腺癌方面具有独特的优势。
礼来的阿贝西利最初于2017年9月28日在美国获批,用于治疗某些类型的HR+/HER2-晚期或转移性乳腺癌。2021年10月13日,FDA批准了阿贝西利的新适应症,联合内分泌治疗用于HR+/HER2-、淋巴结阳性、高复发风险的早期乳腺癌(EBC)成人患者的辅助治疗,并且要求这部分患者的Ki-67(一种细胞增殖标志物)≥20%。
2023年3月3日,FDA进一步扩大了阿贝西利的适应症,取消了Ki-67评分的要求,使得更多HR+/HER2-的高风险早期乳腺癌患者能够使用该药物治疗。
得益于其适应症的扩展和市场需求的增加,阿贝西利的销售额在过去几年中持续增长,尤其是在2022年和2023年,2021年,阿贝西利的全球销售额约为13.5亿美元,同比增长48%;2022年,销售额增长至约24.84亿美元,同比增长约84%;2023年,阿贝西利的销售额达到38.63亿美元,同比增长56%。
推荐阅读
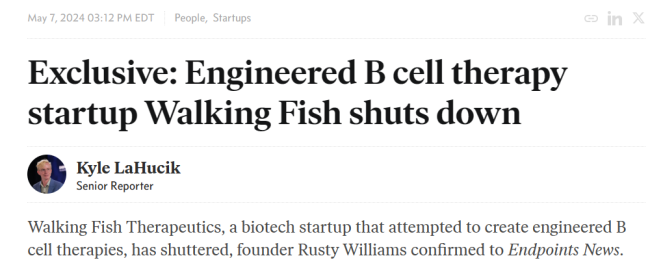
又一家细胞疗法公司倒闭
5月7日,据外媒Endpoint报道,工程化B细胞疗法初创公司Walking Fish Therapeutics(WFT)已经关闭。
裁员互撕,2024年,医药人“倒霉让人心疼”
2022年,生物医药行业露了下行的苗头;2023年,裁员潮开始;2024年,下行不但没有结束,还有了愈演愈烈的意思。
创新药新政没激起水花?Biotech企业:力度太小
过去一周时间里,多则创新药产业链“指南”没能在二级市场激起太大的水花,令不少行业参与者心寒:创新药板块已经没人关注了?
医药板块毛利率双降,发力高端仿制药能成功吗?
花园生物发布2023年业绩报告,公司在2023年实现营收10.95亿元,同比下降22.78%;归母净利润1.92亿元,同比下降49.87%。